 Por Qué Pasa de La Tercera
Por Qué Pasa de La TerceraCientíficos de Stanford logran revertir deterioro cognitivo del alzhéimer con fármaco usado para el cáncer
Los investigadores descubrieron que al bloquear una enzima específica llamada indol-2,3-dioxigenasa 1 (IDO1), podrían rescatar la memoria y la función cerebral en males neurodegenerativos como el alzhéimer.
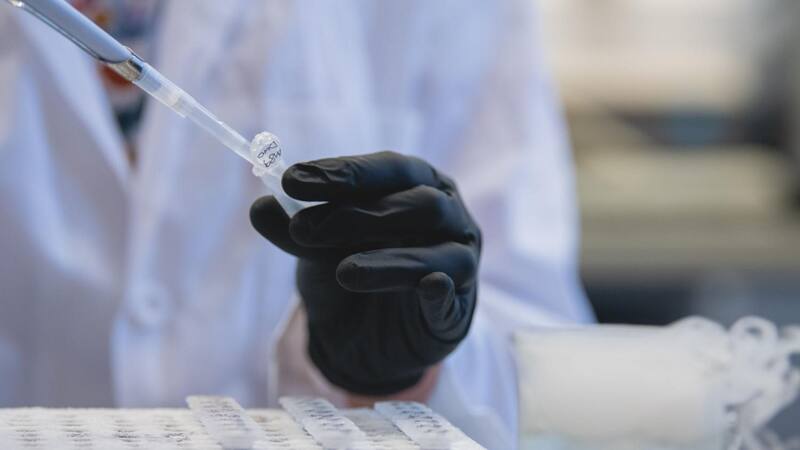
Un tipo de fármaco desarrollado para tratar el cáncer podría transformarse en un prometedor tratamiento para enfermedades neurodegenerativas como el alzhéimer.
Así lo creen científicos de investigadores de la U. Penn State, la Universidad de Stanford junto a un equipo internacional de colaboradores, quienes realizaron un estudio publicado el 22 de agosto en la revista Science.
Científicos de Stanford logran revertir deterioro cognitivo del alzhéimer con fármaco usado para el cáncer
Los investigadores descubrieron que al bloquear una enzima específica llamada indol-2,3-dioxigenasa 1 (que se abrevia IDO1), podrían rescatar la memoria y la función cerebral en modelos que imitan la enfermedad de Alzheimer.
La investigación sugieren que los inhibidores de IDO1 que se están desarrollando actualmente como tratamiento para muchos tipos de cáncer, incluidos el melanoma, la leucemia y el cáncer de mama, podrían reutilizarse para tratar las primeras etapas de las enfermedades neurodegenerativas, una novedad para las enfermedades crónicas que carecen de tratamientos preventivos.
“Estamos demostrando que existe un gran potencial para que los inhibidores de IDO1, que ya están dentro del repertorio de fármacos que se están desarrollando para los tratamientos contra el cáncer, se orienten hacia el tratamiento del alzhéimer”, afirmó en un comunicado la coautora del artículo. Melanie McReynolds.

“En el contexto más amplio del envejecimiento, el deterioro neurológico es uno de los principales cofactores de la incapacidad de envejecer de forma más saludable. Los beneficios de comprender y tratar el deterioro metabólico en los trastornos neurológicos afectarán no solo a quienes reciben el diagnóstico, sino también a nuestras familias, nuestra sociedad y toda nuestra economía”.
La enfermedad de Alzheimer es el tipo más común de demencia, un término general que se refiere a todos los trastornos neurodegenerativos asociados con la edad, explicó McReynolds.
En Chile, se estima que entre un 60% a 80% de los casos de personas con ese diagnóstico corresponde a alzhéimer.
De acuerdo con el último Informe de Estadísticas Vitales del INE, más de 200 mil personas tienen algún tipo de demencia en nuestro país, siendo el alzhéimer el más común. En 2020, la fecha de registro más reciente, murieron 2.180 personas a causa de esta enfermedad: 698 hombres y 1.482 mujeres.
“Inhibir esta enzima, particularmente con compuestos que han sido previamente investigados en ensayos clínicos humanos para el cáncer, podría ser un gran paso adelante en la búsqueda de formas de proteger nuestros cerebros del daño causado por el envejecimiento y la neurodegeneración”, dijo Katrin Andreasson, autora principal del estudio.
La enfermedad de Alzheimer afecta las partes del cerebro que controlan el pensamiento, la memoria y el lenguaje, como resultado de la pérdida progresiva e irreversible de sinapsis y circuitos neuronales.
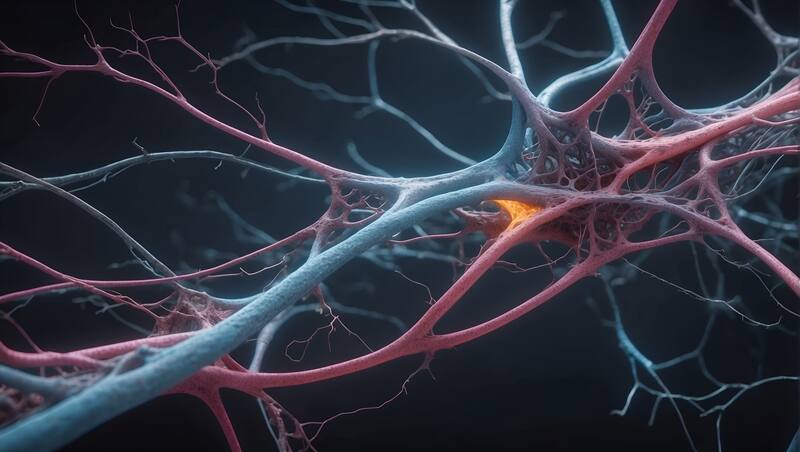
A medida que la enfermedad progresa, los síntomas pueden aumentar desde una leve pérdida de memoria hasta la pérdida de la capacidad de comunicarse y responder al entorno. Los tratamientos actuales para la enfermedad se centran en controlar los síntomas y ralentizar la progresión, mediante la acción sobre la acumulación de placas de amiloide y tau en el cerebro, pero no existen tratamientos aprobados para combatir la aparición de la enfermedad, dijo McReynolds.
“Los científicos han estado trabajando en los efectos secundarios de lo que identificamos como un problema con la forma en que el cerebro se alimenta a sí mismo”, dijo Praveena Prasad , estudiante de doctorado en Penn State y coautora del artículo.
“Las terapias que están disponibles actualmente están trabajando para eliminar péptidos que probablemente sean el resultado de un problema mayor que podemos abordar antes de que esos péptidos puedan comenzar a formar placas. Estamos demostrando que al abordar el metabolismo del cerebro, no solo podemos ralentizar, sino revertir la progresión de esta enfermedad”.
Así funciona el potencial fármaco para tratar el alzhéimer
Utilizando modelos preclínicos (modelos celulares in vitro con proteínas amiloide y tau, modelos de ratón in vivo y células humanas in vitro de pacientes con Alzheimer), los investigadores demostraron que detener la IDO1 ayuda a restablecer el metabolismo saludable de la glucosa en los astrocitos, las células cerebrales en forma de estrella que brindan apoyo metabólico a las neuronas.
La IDO1 es una enzima que descompone el triptófano, la misma molécula presente en el pavo que puede producir sueño, en un compuesto llamado quinurenina.
La producción de quinurenina en el cuerpo es la primera parte de una reacción en cadena conocida como vía de la quinurenina, o KP, que desempeña un papel fundamental en la forma en que el cuerpo proporciona energía celular al cerebro.
Los investigadores descubrieron que cuando la IDO1 generaba demasiada quinurenina, reducía el metabolismo de la glucosa en los astrocitos, que era necesario para alimentar a las neuronas. Al suprimir la IDO1, el apoyo metabólico a las neuronas aumentaba y se restablecía su capacidad de funcionamiento.
Los investigadores llevaron a cabo el estudio en varios modelos de patología de Alzheimer, concretamente la acumulación de amiloide o tau, y descubrieron que los efectos protectores del bloqueo de IDO1 se extienden a estas dos patologías diferentes.
Sus hallazgos sugieren que IDO1 también puede ser relevante en enfermedades con otros tipos de patología, como la demencia o el Parkinson, así como el amplio espectro de trastornos neurodegenerativos progresivos conocidos como tauopatías, explicó Paras Minhas, primer autor del artículo.
“El cerebro depende en gran medida de la glucosa para alimentar muchos procesos, por lo que perder la capacidad de utilizar eficazmente la glucosa para el metabolismo y la producción de energía puede provocar un deterioro metabólico y, en particular, un deterioro cognitivo”, afirmó Minhas.
“A través de esta colaboración pudimos visualizar con precisión cómo el metabolismo del cerebro se ve afectado por la neurodegeneración”.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
2.
3.
¿Vas a seguir leyendo a medias?
Todo el contenido, sin restriccionesNUEVO PLAN DIGITAL $1.990/mes SUSCRÍBETE
















