Miércoles de evaluaciones en el ISP: mañana revisará autorización para uso excepcional de vacuna Sinovac y en siete días más será turno de Astrazeneca
A las 9 de la mañana se inicia reunión clave que decidirá próxima vacunación en el país.
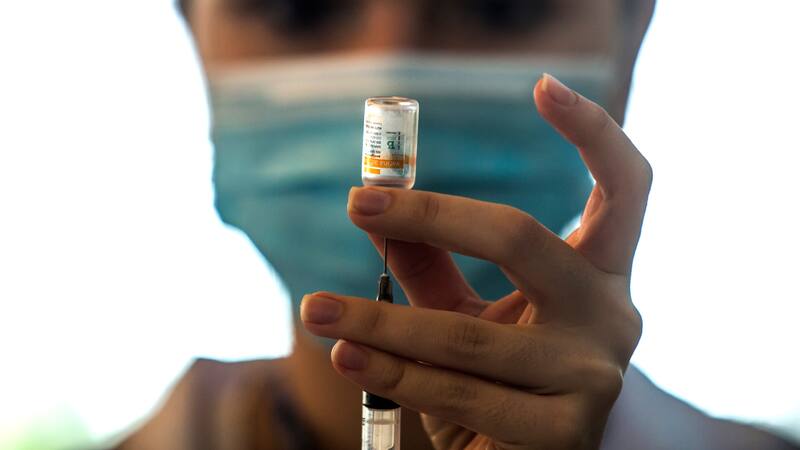
A las 9 de la mañana, el Instituto de Salud Pública (ISP) y el comité de expertos decidirán un permiso extraordinario pata que la vacuna china de Sinovac Biotech contra Covid-19 pueda ser utilizada en el país.
Como la farmacéutica china no tiene representación en el país, el pasado 28 de diciembre, la Central Nacional de Abastecimiento (Cenabast) presentó ante el ISP una solicitud de probación excepcional, trámite que tenía como plazo 15 días para su evaluación.
Al igual como ocurrió con la autorización de Pfizer el 16 de diciembre pasado, se realizará una reunión que será transmitida de manera on line para mayor transparencia.
“Mañana lo que haremos es el resumen de las presentaciones de todo lo que se revisó y evaluó de Sinovac para presentación del comité y que éste recomiende si la seguridad calidad y eficacia de la vacuna es adecuada para su aprobación. Como director, tomaré esas recomendaciones y haré la decisión correcta con respecto de lo que necesitamos en vacunas en Chile”, señala el director (s) del ISP, Heriberto García.
La subsecretaria de Salud, Paula Daza, dice que se espera tener esta vacuna a fines de enero o los primeros días de febrero “cuando empiecen a llegar los cargamentos, siempre y cuando tengamos la aprobación del ISP”. Con esta farmacéutica, Chile tiene un contrato por cera de 10 millones de vacunas.

El comité de expertos está constituido en total por 16 funcionarios del ISP y seis externos (médico Internista intensivista de la UC, un médico Pediatra Broncopulmonar de la UDD, un químico farmacéutico doctorado de la U. de Valparaíso, otro de la Universidad Austral, otro doctorado sin filiación, un médico Internista Oncólogo de Clínica Indisa, un médico pediatra infectólogo del Depto. de Inmunizaciones del Ministerio de Salud y otro médico pediatra infectólogo del Comité Asesor de Vacunas (Cavei).
Desde el ISP, el equipo estará encabezado por el director, el jefe del Departamento de Anamed, jefe de Autorizaciones y Registro de Productos Nuevos y Biológicos, la jefa de Farmacovigilancia, jefe de sección de Estudios Clínicos, jefa de Sección de Registro de Productos Biológicos, jefe Sección de Biotecnología. químico farmacéuticos de la Sección Registro de Productos Biológicos y otros profesionales químicos farmacéuticos.
Esta vacuna, ya obtuvo la autorización de importación por lo que se espera que las primeras dosis lleguen a partir de la próximas semana. De aprobarse su autorización de uso, se podrá iniciar la vacunación de la población.
Resultados
La semana pasada, Brasil dio a conocer los primeros resultados del estudio Fase 3 que están realizando y en el que participaron 16 centros de investigación científica en siete estados más el Distrito Federal, con 12.500 profesionales de la salud como voluntarios.
De acuerdo a estos cifras, la vacuna protege de desarrollar casos moderados y graves de la enfermedad. Los casos leves (casi sin síntomas) mostraron una efectividad de 77,96% y los casos moderados y graves fue del 100%. Es decir, la vacuna logró que entre las personas vacunadas el 49,7% reportara síntomas muy leves que pudieron pasar en casa, el 22% un cuadro leve que requiere algún tipo de asistencia (77.96% de eficacia) y ninguno (100% de eficacia) requirió hospitalización, ni oxígeno, es decir no se registró ningún caso grave entre quienes recibieron la vacuna.

Adultos mayores
La vacuna de Sinovac ya ha demostrado ser segura para los adultos mayores en los estudios Fase 2 y Fase 2 que se han realizado.
En Chile, investigadores de la UC están realizando los estudios clínicos fase 3 y continúan con el reclutamiento de voluntarios.
Susan Bueno, profesora de la Facultad de Ciencias Biológicas de la UC, investigadora del Instituto Milenio en Inmunología e Inmunoterapia (IMII) y directora Científica del Estudio Clínico Fase 3 en Chile de la Vacuna de Sinovac, señala que en el protocolo del estudio hay participación de adultos mayores, sin límite de edad para participar.
“Esperamos en este estudio contar con un número suficiente de personas mayores de 60 años que permitan hacer análisis robustos sobre la respuesta inmune inducida por la vacuna en este grupo poblacional, así como en jóvenes. La evaluación de la respuesta inmune de personas mayores de 60 años a la vacuna es de especial interés para todos y puede contribuir a lineamientos de vacunación que realizará el Ministerio de Salud, al contar con evidencia científica de primera fuente y local para determinar la capacidad de la vacuna de inducir inmunidad protectora de larga duración”, indica.
Pablo González, académico de la UC, investigador del IMII y director ejecutivo del estudio, dice que hasta ahora el proceso de reclutamiento ha avanzado satisfactoriamente y ya cuentan con un importante número de personas interesadas en participar, que se han inscrito a través de la página web del estudio, que serán prontamente enrolados. Los interesados en participar pueden inscribirse en la página web oficial de este estudio clínico www.coronavacfase3.cl.
Se estima que el estudio seguirá hasta que se complete el número total de sujetos contemplados, lo que ocurriría en las próximas 6 y 10 semanas.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
2.
3.
¿Vas a seguir leyendo a medias?
Todo el contenido, sin restriccionesNUEVO PLAN DIGITAL $1.990/mes SUSCRÍBETE

















