Por Qué Pasa de La Tercera
Por Qué Pasa de La TerceraMini corazones cultivados en laboratorio laten como si fueran reales
Los órganos en miniatura, u organoides, imitan el corazón en funcionamiento de un embrión humano de 25 días y podrían ayudar a desentrañar muchos misterios, incluido por qué los corazones de los bebés no dejan cicatrices después de sufrir un ataque cardíaco.
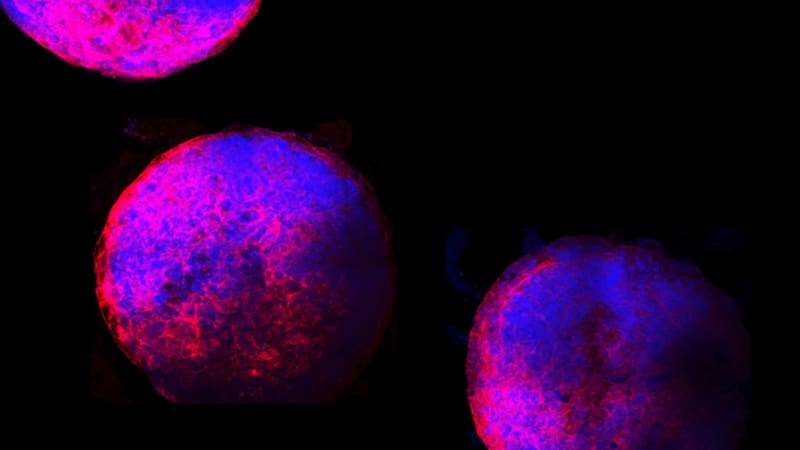
No son más grandes que las semillas de sésamo y pulsan con un ritmo hipnótico. Estos son “minicorazones” humanos, los primeros que se crearon en el laboratorio con cámaras que palpitaban claramente.
“Este es un gran estudio”, indicó Zhen Ma, un bioingeniero que desarrolla organoides cardíacos en la Universidad de Syracuse en Nueva York. El experimento es “muy importante” para comprender los defectos cardíacos congénitos y la formación del corazón humano, un trabajo que hasta ahora se ha basado en modelos animales, señaló el bioingeniero.
Aunque los “miniorganos” como el cerebro, las tripas y el hígado se han cultivado en platos durante más de 10 años, los organoides del corazón han sido más desafiantes. Los primeros, compuestos por células cardíacas de ratón, podían contraerse rítmicamente en un plato, pero parecían más un bulto de células cardíacas que un corazón adecuado, dice Aitor Aguirre, biólogo de células madre de la Universidad Estatal de Michigan que ha creado su propio organoide de corazón humano, descrito en una preimpresión publicada en Research Square. “Un organoide debe recapitular la función del órgano. Con un corazón, esperarías cámaras y bombeo, porque esto es lo que hace el corazón”, señala.
Para crear organoides cardíacos cuyas células se autoorganizan como las de un embrión, los autores del nuevo estudio programaron células madre pluripotentes humanas, que tienen la capacidad de diferenciarse en cualquier tipo de tejido en varios tipos de células cardíacas. Su objetivo era crear las tres capas de tejido presentes en las paredes de una cámara cardíaca, una de las primeras partes del corazón en desarrollarse. A continuación, los investigadores sumergieron las células madre en diferentes concentraciones de nutrientes promotores del crecimiento hasta que encontraron una receta que inducía a las células a formar tejidos en el mismo orden y forma que se ven en los embriones.
Después de 1 semana de desarrollo, los organoides son estructuralmente equivalentes al corazón de un embrión de 25 días. En esta etapa, el corazón tiene solo una cámara, que se convertirá en el ventrículo izquierdo del corazón maduro. Los organoides miden aproximadamente 2 milímetros de diámetro e incluyen los principales tipos de células típicamente presentes en esta etapa de desarrollo: cardiomiocitos, células epiteliales, fibroblastos y epicardio. También tienen una cámara claramente definida que late de 60 a 100 veces por minuto, la misma frecuencia del corazón de un embrión alrededor de la misma edad, informó el equipo en la revista científica Cell.
“Cuando lo vi por primera vez, me sorprendió que estas cámaras pudieran formarse por sí mismas”, mencionó la autora principal Sasha Mendjan, bióloga de células madre del Instituto de Biotecnología Molecular de la Academia de Ciencias de Austria. “Lo sorprendente es que ves inmediatamente si el experimento funcionó y el organoide es funcional, ya que late, a diferencia de otros órganos”.
Los mini corazones, que hasta ahora han sobrevivido durante más de 3 meses en el laboratorio, ayudarán a los científicos a ver el desarrollo del corazón con un detalle sin precedentes. También podrían revelar el origen de problemas cardíacos como defectos cardíacos congénitos en bebés y muerte de células cardíacas después de ataques cardíacos, dice Mendjan. “No se puede entender completamente algo hasta que se puede volver a crear”, sostuvo Mendjan, parafraseando al físico Nobel Richard Feynman.
Mendjan y sus colegas también congelaron trozos de organoides para probar su respuesta a las lesiones. Vieron que los fibroblastos cardíacos, un tipo de célula responsable de mantener la estructura del tejido, migraban a las áreas dañadas para reparar las células muertas, al igual que en los bebés que experimentan ataques cardíacos. Durante mucho tiempo ha sido un misterio por qué los corazones de los bebés pueden regenerarse después de tal lesión sin dejar cicatrices, a diferencia de los adultos. “Ahora, tenemos un sistema limpio y controlado fuera del cuerpo humano para estudiar fácilmente este proceso”, agregó Mendjan.
Aguirre mencionó que el siguiente paso lógico es conectar los organoides del corazón latiendo a las redes vasculares y probar su capacidad para bombear sangre. El equipo de Mendjan planea intentar ajustar el caldo de nutrientes para producir organoides con las cuatro cámaras. Con organoides cardíacos tan avanzados, los investigadores podrían explorar los muchos problemas cardíacos del desarrollo que surgen cuando estas cavidades adicionales comienzan a formarse.
Para Ma, cultivar un organoide cardíaco más adulto, con todas sus cámaras y estructuras, es el futuro del campo. Pero no cree que esto suceda en la próxima década. Para un organoide completo con forma de corazón, explicó, “todavía queda un largo camino por recorrer”.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
Casi nadie tiene claro qué es un modelo generativo. El resto lo leyó en La Tercera
Plan Digital + LT Beneficios$6.990 al mes SUSCRÍBETE