 Por Cristina Pérez
Por Cristina PérezNiños en EEUU reciben inyección contra distrofia muscular gracias a hallazgos de científicos chilenos
La terapia que buscan validar en Estados Unidos permitiría frenar el avance de la enfermedad de Duchenne, gracias al trabajo realizado por casi dos décadas de un grupo de investigadores chilenos liderados por el doctor Enrique Brandán.
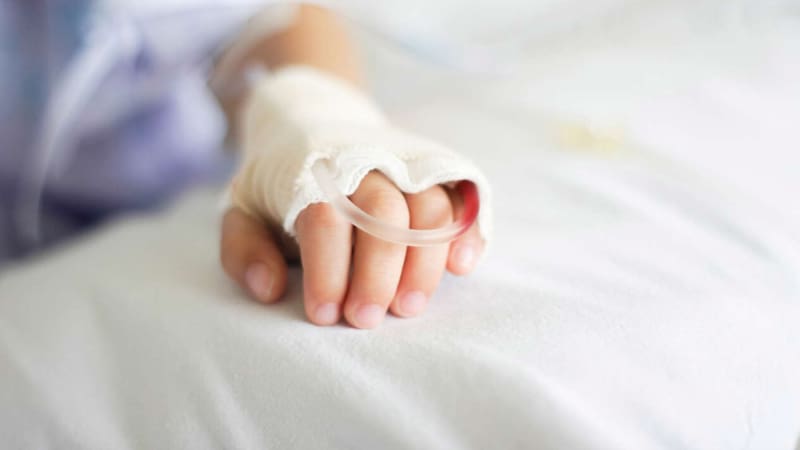
La enfermedad de Duchenne es una forma de distrofia muscular que empeora rápidamente (otras, como la enfermedad de Becker, lo hacen mucho más lentamente). Es causada por un gen defectuoso para la distrofina (una proteína en los músculos), que se transfiere de forma hereditaria y está ligada al cromosoma X, o sea que solo se presenta en niños varones.
Se trata, de un apatología de baja frecuencia, comúnmente llamada “enfermedad rara” de más alta incidencia a nivel internacional. En Chile, por ejemplo, se calcula que afecta actualmente a unas mil personas, aunque no existen catastros oficiales, y no existen alternativas terapéuticas curativas ni capaces de controlar la enfermedad.
La primera manifestación clínica, es un retraso en el desarrollo locomotor (dificultad de marcha) y posteriormente para correr, subir escalas o saltar debido a una gran debilidad muscular.
Pero, la firma norteamericana FibroGen culminó el proceso de reclutamiento de 183 pacientes diagnosticados (niños y adolescentes de sexo masculino) con distrofia muscular de Duchenne que participan en dos estudios clínicos simultáneos en fase 3.
Esto luego de los prometedores resultados obtenidos en la fase 2 y que permitirán evaluar una terapia experimental basada en hallazgos formulados por científicos chilenos. El desarrollo consiste en la inyección de un anticuerpo que bloquea la fibrosis muscular esquelética asociada a las distrofias musculares.
Los descubrimientos iniciales fueron liderados desde el año 2006 por el Dr. Enrique Brandán, actual investigador del Centro Basal ANID Ciencia y Vida.
El científico trabaja desde hace casi dos décadas en esta enfermedad, realizando importantes descubrimientos, especialmente sobre las moléculas que inducen la fibrosis y sus respectivos inhibidores, los que se están utilizado en nuevos estudios, como el que hoy se desarrolla en Estados Unidos.
Los ensayos –que se realizan en varias ciudades de EE.UU.– buscan validar la efectividad y seguridad de este desarrollo biotecnológico, previamente evaluados en modelos de animales. Su administración podría frenar el avance progresivo y mortal de esta condición, que es diagnosticada en niños de sexo masculino, con una prevalencia de uno entre aproximadamente 3.500 nacimientos.
El Dr. Brandan destacó que estos estudios se realizan como parte de una iniciativa “fast track” o de vía rápida impulsada por la FAgencia de Drogas y Medicamentos de EE.UU (FDA, su sigla en inglés), la agencia reguladora e fármacos de Estados Unidos), lo que permitiría en el mejor de los casos tener la aprobación de la droga en mayo de 2024, lo que también posibilitaría transferir al mercado el fármaco dentro del mismo año.
Para las enfermedades más comunes y de mayor incidencia, como la gripe, la hipertensión o la artritis, ya casi no se están llevando a cabo estudios clínicos, porque ya tienen un número significativo de drogas efectivas.
Por lo anterior, “se han dado incentivos especiales para la búsqueda de drogas que puedan tratar estas enfermedades raras”, aunque el Dr. Brandan recalca que el mal tampoco es tan “raro” pues la distrofia muscular de Duchenne tiene una incidencia importante, en alrededor de uno en 3.500 nacimientos.
Niños reciben droga basada en hallazgos de científicos chilenos
La contribución del laboratorio nacional en la búsqueda de alternativas terapéuticas contra la distrofia muscular de Duchenne no se reduce a los ensayos que se efectúan en Estados Unidos. Una reciente publicación en la revista Matrix Biology –de elevado impacto científico– demostró nuevos hallazgos del laboratorio chileno en relación con esta patología.
En particular, el descubrimiento de un eje de moléculas que inducen fibrosis y sus respectivos inhibidores ha dado pie al inicio de un nuevo estudio financiado por Fondecyt, y que apunta a determinar nuevas moléculas que bloqueen la respuesta fibrótica de la enfermedad.
Dicha línea podría contribuir a adelantar el inicio de los tratamientos a una fase donde los niños aún tengan capacidad de autonomía, predictora de la fase crítica y con peor calidad de vida del síndrome.
El Dr. Brandan detalla que, en estas enfermedades, la proteína distrofina y una segunda, llamada sarcoglicán (vinculada al nuevo estudio), se encuentran ausentes, evitando que se genere la fuerza en las fibras musculares.
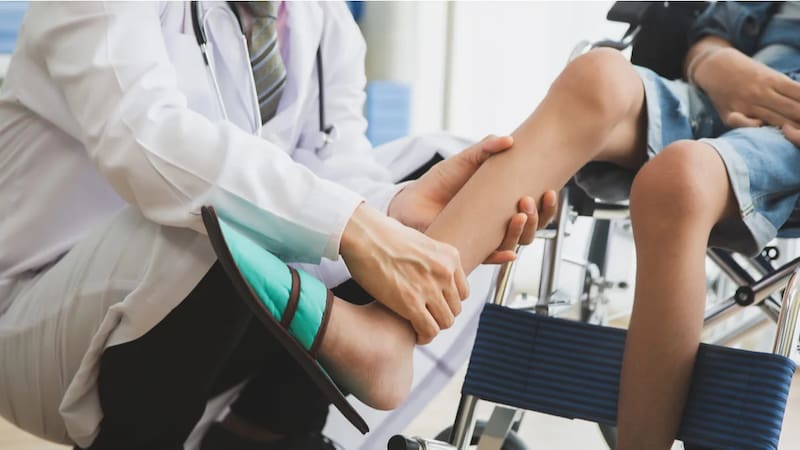
Es, en definitiva, un problema a nivel celular, que evita que la contracción de la fibra se traduzca en una fuerza efectiva. Al no estar presentes alguna de estas proteínas el complejo por el que se transmite la fuerza se desarma, evitando que esa energía sea transmitida a través de la matriz extracelular, una estructura que rodea la célula muscular. La distrofina y la sarcoglicán son dos de aproximadamente diez proteínas que conforman este complejo.
Avances contra este tipo de distrofia muscular
De acuerdo al Ministerio de Salud, que dispone de una norma técnica para evaluar científicamente en Chile alternativas terapéuticas para condiciones de este tipo, la distrofia muscular de Duchenne es una “enfermedad incurable”. Por esto, los tratamientos o intervenciones que se analizan para financiamiento y aprobación a nivel local se definen como “ayudas técnicas”.
A la edad de 12 años, la mayoría de los niños varones con esta enfermedad necesitan utilizar una silla de ruedas. La debilidad progresiva de los músculos respiratorios también los hace especialmente vulnerables ante la neumonía y otras enfermedades y la mayoría de ellos mueren hacia los 30 años de edad.
La terapia que buscan validar en Estados Unidos a través de estos ensayos, liderada por la firma FibroGen y propiciada por estudios realizados por investigadores chilenos, no permitiría revertir el síndrome, sino frenar su avance. Todo esto, advierte el Dr. Brandan, mientras la nueva generación de desarrollos biotecnológicos emergentes, entre ellos el de edición genética beneficie a estos pacientes. La más relevante de ellas es el método CRISPR.
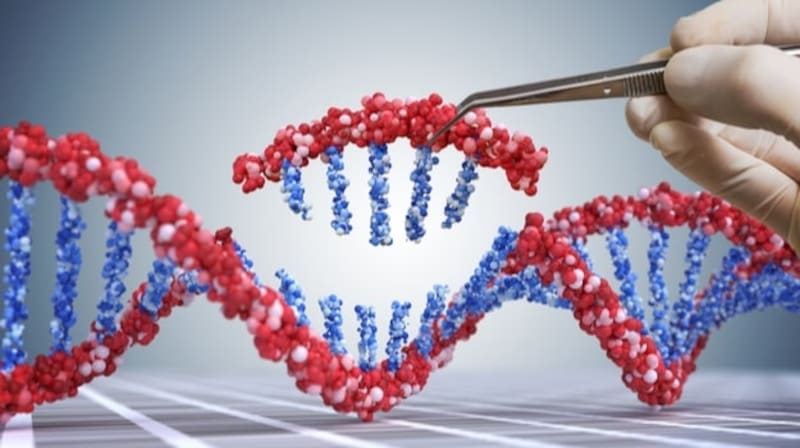
“Duchenne es una enfermedad genética que por ahora no tiene cura. Todo cambia muy rápido y ya hay trabajos muy prometedores en modelos animales con técnicas de edición genética, donde es posible reparar las células musculares de nuestro cuerpo, las mutaciones, casi como ciencia ficción. Es una metodología nueva, aunque más investigación se requiere para ver si son seguras y estables en el tiempo”, añade el investigador chileno.
La edición genética que podría curar Duchenne permitiría que, a través de una inyección, se intervenga el ADN de las billones de células del cuerpo humano y reparar las mutaciones, algo que en el caso de la distrofia muscular sería especialmente desafiante: habría que llegar a todos los músculos (son más de 600) y editar su ADN. De momento, entonces, no hay soluciones definitivas.
“Si me hubiesen preguntado hace 15 años, habría dicho que la cura se encontraría antes del 2018, pero todo indica que tomará aún más tiempo”, comenta Brandan.
Nuevo estudio para estudiar más detalles de esta distrofia muscular
A la espera de la evolución de la industria biotecnológica y también de los numerosos estudios que podrían dar esperanzas de una mejor calidad de vida a los pacientes, el grupo liderado por el investigador de la fundación Ciencia y Vida, apuesta por explorar opciones distintas.

Un recién terminado proyecto de investigación abrió una nueva línea de investigación que podría ser importante en este campo, principalmente por el tiempo de administración.
“El proyecto Fondecyt que comenzamos tiene como objetivo final poder encontrar nuevas moléculas que inhiban la respuesta fibrótica e inflamatoria en modelos de distrofia muscular, estamos proponiendo un modelo, y vamos a usar un modelo de ratón distinto al modelo de distrofia muscular de Duchenne es un modelo que presenta similitudes, pero presenta la ventaja experimental que genera síntomas muy tempranos” explica el especialista.
“Eso significa que podemos comenzar a dar drogas desde antes de los síntomas más severos”, enfatizó el científico chileno.
La respuesta fibrótica es la forma que encuentra el músculo de cicatrizar el tejido que no es capaz de producir la contracción muscular. Es una respuesta reparadora ante la mutación genética que ocasiona la producción de proteína distrofina, en el caso de Duchenne, clave para la estructura y función muscular. El nuevo proyecto Fondecyt apunta a seguir explorando esta respuesta fibrótica, asociadas a distrofias musculares.
Niños en EEUU reciben inyección gracias a Medicina traslacional
La probabilidad de hacer medicina traslacional, es decir, de transferir avances desde el laboratorio hacia el paciente, en un proceso que comienza con estudios en ciencia básica, hasta finalmente traspasarlos al mercado, tras años de diversos estudios clínicos en distintas poblaciones de seres humanos, es baja. Más aún desde Chile, donde el financiamiento para la investigación y desarrollo es uno de los más bajos entre los países en vías de desarrollo.
Sin embargo, el trabajo liderado por el Dr. Brandan en los últimos años constituye una excepción.
“No es común que lo que uno descubra pueda servir para tratar enfermedades, que es lo que ha ocurrido acá, donde nos hemos visto apoyados por una serie de circunstancias, de suerte o azar para pasar del mesón al paciente. Ninguno de los hitos que hoy vemos podría haber ocurrido sin las pruebas de conceptos iniciales realizadas en nuestro laboratorio, como que la empresa que tenía los anticuerpos contra la fibrosis se haya interesado por nuestro estudio”.
El actual investigador del Centro Basal Ciencia y Vida y la Universidad San Sebastián comentó que como parte de las exploraciones que ha realizado en los últimos años ha materializado acercamiento con agrupaciones de pacientes –que reúnen a familias de niños diagnosticados– de Duchenne, como la Fundación Duchenne Chile, con el propósito de crear consciencia sobre la enfermedad y la necesidad de avanzar en su comprensión y espacios de inclusión.
Esto lo ha motivado de manera personal y también a su equipo de trabajo.
“Es una enfermedad tremenda, que no distingue clases sociales. Ha sido una parte muy gratificante de mi carrera como científico, en la cual no pensé participar. Hemos dado charlas a profesores y padres. Y nos dimos cuenta los problemas que tenían en los colegios. Entonces comenzamos a dar charlas también en colegios, a profesores, directores, comunidad escolar, etc. El objetivo era sensibilizar sobre problemas comunes de los niños y que muchas veces a las familias era difícil poder transmitir”.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
3.
4.
¿Vas a seguir leyendo a medias?
Todo el contenido, sin restriccionesNUEVO PLAN DIGITAL $1.990/mes SUSCRÍBETE


















