Prometedora vacuna china contra el coronavirus será probada en Chile
Laboratorio Sinovac Biotech espera producir 100 millones de dosis al año para combatir el virus Sars-CoV-2. La alianza permitirá que en caso de resultar exitosa, el país tenga facilidades de acceso a la vacuna.
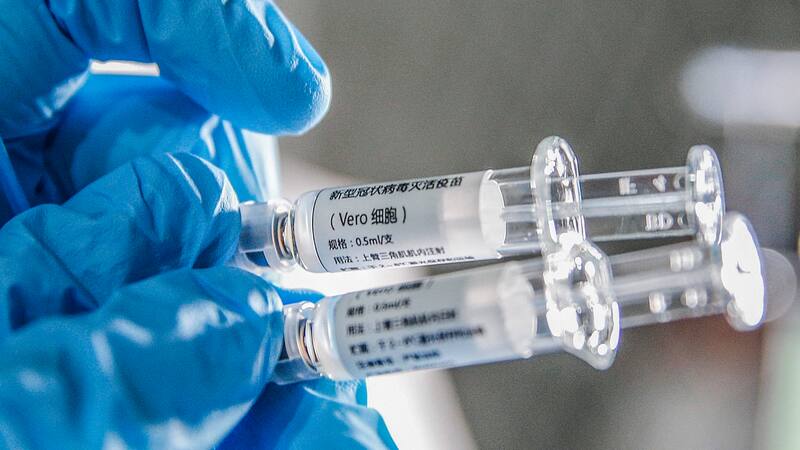
Un convenio de colaboración con la biofarmacéutica china Sinovac Biotech permitirá que Chile participe del estudio clínico que evaluará una de las vacunas contra el coronavirus Sars-CoV-2 que más adelantada está en su investigación y desarrollo.
Se trata de una alianza de colaboración entre la Pontificia Universidad Católica, a través del Instituto Milenio de Inmunología e Inmunoterapia (IMII) y la empresa biofarmacéutica china.
La compañía fundada de 2001, fue el primer laboratorio en desarrollar una vacuna contra la gripe porcina H1N1 en el año 2009 y hoy es uno de los cuatro laboratorios chinos autorizados para realizar ensayos clínicos que permitan un tratamiento de inmunización para proteger a la población del Covid-19.
En abril, Sinova Biotech anunció resultados positivos con esta formulación en pruebas realizadas en monos y actualmente conduce estudios clínicos un gran número de participantes en China.
En las próximas tres semanas, iniciará estudios en Fase 3 con voluntarios de Brasil y tal como ha indicado el laboratorio, cuando terminen las pruebas clínicas en humanos, esperan producir 100 millones de dosis al año.
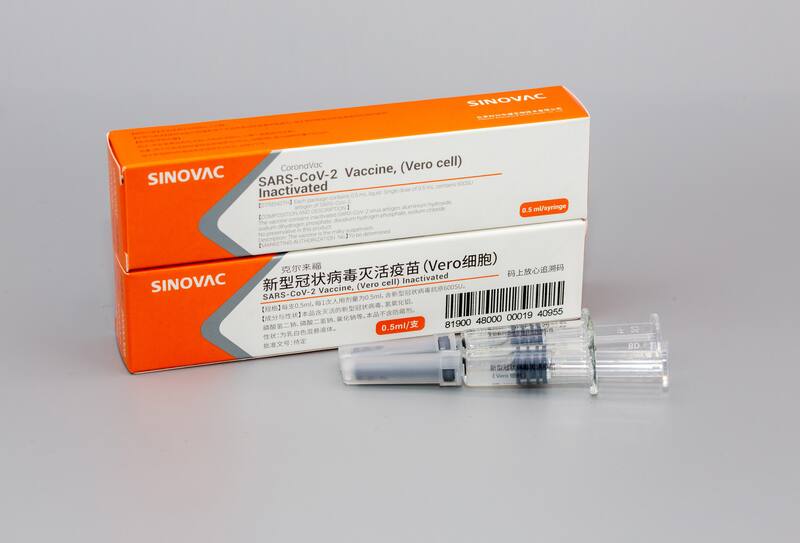
Alexis Kalergis, académico de la UC y director ejecutivo de IMII señala que los resultados clínicos que ha tenido hasta ahora la vacuna china son muy favorables, “se percibe como una vacuna segura y eventualmente, eficaz”, dijo.
Esta alianza también permitirá acercar la ciencia chilena a la ciencia que realizan países del primer mundo y que ellos también conozcan el trabajo que se realiza en el país.
Si bien los resultados de la fase I y II de CoronaVac ya se hicieron, aún falta revisarlos bien y de acuerdo a eso, diseñar una Fase III para que pueda ser realizada en Chile en los próximos meses.
Susan Bueno, profesora de la Facultad de Ciencias Biológicas de la Universidad Católica e investigadora del Instituto Milenio de Inmunología e Inmunoterapia (IMII), explica que de cumplir con todos los parámetros de seguridad e inmunogenicidad en las fases 1 y 2 realizadas anteriormente, se podría iniciar la fase clínica III.
“Este tipo de estudio clínico evalúa la efectividad de la vacuna, es decir, si la vacuna es capaz de proteger a los vacunados contra la enfermedad. Por lo tanto, estos estudios incluyen a un número importante de participantes adultos sanos en quienes se evalúa si la vacuna protegió contra la enfermedad”, señala la investigadora.
Vacunas para Chile
Para la elaboración del protocolo que entregará los marcos para el estudio de Fase III, se considera la población sobre la que se estudiará, la tasa de infección en la localidad donde se desarrolla el estudio clínico y cómo se evaluará la capacidad de protección de la vacuna, entre otros aspectos. “Actualmente hay avances en el diseño del estudio clínico Fase 3, así como respecto a qué lugares podrían participar, pero es trabajo en progreso. Podrían ser miles de potenciales voluntarios chilenos los que participen”, dice Bueno.
La realización de en estudios clínicos permitirá a Chile participar en los análisis de efectividad de la vacuna contra el Covid-19, lo que facilita el acceso de nuestro país a la vacuna.
“Es importante explorar múltiples caminos de acción para garantizar el acceso a una vacuna. Uno de éstos, sin duda, es el desarrollo en Chile de investigación científica para la generación de prototipos locales, dado que eso nos posiciona en el mapa de desarrolladores de vacunas”, dice Kalergis.
Además, agrega que la colaboración con grupos y organismos internacionales es clave, porque de esa manera se puede “conocer y acceder de primera fuente a los avances hechos por otros equipos”. “Adicionalmente, a nivel internacional se han emitido múltiples declaraciones relacionadas a la necesidad de liberar los derechos de propiedad intelectual y facilitar el licenciamiento de productos claves para abordar y posiblemente resolver la pandemia causada por Covid-19”, indicó.
COMENTARIOS
Para comentar este artículo debes ser suscriptor.
Lo Último
Lo más leído
4.


















